Mastiplan® LC 300 mg/20 mg
Suspension zur intramammären Anwendung für Milchkühe
Zusammensetzung
Jeder 8 g Euterinjektor mit Suspension enthält:
Wirkstoff(e):
Cefapirin (als Cefapirin Natrium) 300 mg
Prednisolon 20 mg
Creme-/gelbe bis rosafarbene, ölige, homogene Suspension.
Zieltierart(en)
Rind (Kuh, laktierend)
Anwendungsgebiet(e)
Zur Behandlung klinischer Mastitiden bei laktierenden Milchkühen hervorgerufen durch Cefapirin-empfindliche Staphylococcus aureus, Koagulase-negative Staphylokokken, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis und Escherichia coli.
Gegenanzeigen
Nicht anwenden bei bekannter Überempfindlichkeit gegen Cephalosporine, andere ß-Laktam-Antibiotika oder gegen einen der sonstigen Bestandteile.
Besondere Warnhinweise
Besondere Vorsichtsmaßnahmen für die sichere Anwendung bei den Zieltierarten:
Das Reinigungstuch bei einer bestehenden Zitzenverletzung nicht anwenden.
Die Anwendung des Tierarzneimittels sollte auf der Identifizierung und Empfindlichkeitsprüfung des/der Zielerreger/s basieren. Falls dies nicht möglich ist, sollte die Anwendung auf epidemiologischen Informationen und Kenntnissen zur Empfindlichkeit der Zielerreger auf Bestandsebene oder auf lokaler/regionaler Ebene beruhen. Bei der Anwendung des Tierarzneimittels sind die amtlichen, nationalen und örtlichen Regelungen über den Einsatz von Antibiotika zu berücksichtigen.
Ein Antibiotikum mit einem geringeren Risiko der Resistenzselektion (niedrigere AMEG Kategorie) sollte als Mittel der ersten Wahl zur Behandlung verwendet werden, sofern die Empfindlichkeitsprüfung dessen Wirksamkeit nahelegt. Die Verfütterung der zu verwerfenden Milch mit Cefapirin-Rückständen an Kälber sollte bis zum Ende der Wartezeit auf Milch (außer während der Kolostralphase) vermieden werden, da antimikrobiell resistente Bakterien in der Darmmikrobiota selektiert werden könnten und es zu einer verstärkten fäkalen Ausscheidung dieser Bakterien kommen könnte.
Eine von den Vorgaben der Fachinformation abweichende Anwendung des Tierarzneimittels kann die Prävalenz von Bakterien, die gegen Cefapirin resistent sind, erhöhen und den Behandlungserfolg verringern.
Besondere Vorsichtsmaßnahmen für den Anwender:
Penicilline und Cephalosporine können nach Injektion, Inhalation, oraler Aufnahme oder Hautkontakt zu Überempfindlichkeitsreaktionen (Allergien) führen. Eine Überempfindlichkeit gegenüber Penicillinen kann zu einer Kreuzallergie gegenüber Cephalosporinen führen und umgekehrt. Gelegentlich kann es zu schwerwiegenden allergischen Reaktionen gegenüber diesen Substanzen kommen.
Personen mit bekannter Überempfindlichkeit gegen Cephalosporine, Penicilline oder Prednisolon sollten den Kontakt mit dem Tierarzneimittel vermeiden.
Das Tierarzneimittel ist mit großer Sorgfalt zu handhaben, um einen versehentlichen Kontakt zu vermeiden. Alle empfohlenen Vorsichtsmaßnahmen sind zu berücksichtigen.
Treten nach Exposition klinische Symptome wie z.B. Hautausschlag auf, ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder das Etikett vorzuzeigen. Symptome wie Anschwellen des Gesichtes, der Lippen oder Augenlider sowie Atembeschwerden sind ernst zu nehmen und bedürfen einer sofortigen ärztlichen Versorgung.
Nach Benutzung des Reinigungstuchs Hände waschen. Bei Auftreten von Hautirritationen durch Isopropylalkohol oder bei bekannter Überempfindlichkeit sind Schutzhandschuhe zu tragen.
Trächtigkeit und Laktation:
Das Tierarzneimittel kann während der Laktation angewendet werden.
Laborstudien an Mäusen, Ratten, Kaninchen und Hamstern ergaben keine Hinweise auf teratogene, fetotoxische oder maternotoxische Wirkungen.
Da keine entsprechenden Untersuchungen bei der Zieltierart durchgeführt wurden, sollte bei tragenden oder zur Zucht vorgesehenen Tieren die Anwendung nur nach entsprechender Nutzen-Risiko-Bewertung durch den behandelnden Tierarzt erfolgen.
Wechselwirkung mit anderen Arzneimitteln und sonstige Wechselwirkungen:
Die gleichzeitige Anwendung von bakteriostatischen Antibiotika kann zu antagonistischen Wirkungen führen.
Die gleichzeitige parenterale Verabreichung von Aminoglykosiden oder anderen nephrotoxischen Arzneimitteln wird nicht empfohlen.
Nebenwirkungen
Rind (Kuh, laktierend)
| Sehr selten (< 1 Tier/10 000 behandelte Tiere, einschließlich Einzelfallberichte): | Überempfindlichkeitsreaktion |
Die Meldung von Nebenwirkungen ist wichtig. Sie ermöglicht die kontinuierliche Überwachung der Verträglichkeit eines Tierarzneimittels. Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage aufgeführt sind, bei Ihrem Tier feststellen oder falls Sie vermuten, dass das Tierarzneimittel nicht gewirkt hat, teilen Sie dies bitte zuerst Ihrem Tierarzt mit. Sie können Nebenwirkungen auch an den Zulassungsinhaber unter Verwendung der Kontaktdaten am Ende dieser Packungsbeilage oder über Ihr nationales Meldesystem melden.
Die Meldungen sind vorzugsweise durch einen Tierarzt an das Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL) zu senden. Meldebögen und Kontaktdaten des BVL sind auf der Internetseite https://www.vet-uaw.de/ zu finden oder können per E-Mail (uaw@bvl.bund.de) angefordert werden. Für Tierärzte besteht die Möglichkeit der elektronischen Meldung auf der oben genannten Internetseite.
Dosierung für jede Tierart, Art und Dauer der Anwendung
Der Inhalt eines Injektors wird unmittelbar nach dem Melken alle 12 Stunden an jeweils 4 aufeinander folgenden Melkzeiten vorsichtig in den Zitzenkanal des betroffenen Euterviertels injiziert. Jeder Injektor ist nur einmal für eine Zitze zu verwenden.
Hinweise für die richtige Anwendung
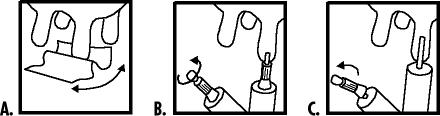
Jedes betroffene Euterviertel vor der Applikation vollständig ausmelken. Zitze und Zitzenöffnung gründlich reinigen und mit dem beigelegten Reinigungstuch desinfizieren (A). Kontaminationen der Injektorspitze vermeiden. Entweder den vorderen kleinen Teil der Kappe abreißen und vorsichtig ungefähr 5 mm in den Zitzenkanal einführen (B) oder die Kappe vollständig entfernen und vorsichtig die gesamte Injektorspitze in den Zitzenkanal einführen (C). Den gesamten Inhalt des Injektors in das Euterviertel verabreichen.
Das Tierarzneimittel durch leichte Massage der Zitze und des Euters des betroffenen Tieres verteilen.
Wartezeiten
| Essbare Gewebe: | 4 Tage (96 Stunden) |
| Milch: | 5,5 Tage (132 Stunden) |
Besondere Lagerungshinweise
Arzneimittel unzugänglich für Kinder aufbewahren.
Die Euterinjektoren im Aluminiumbeutel und im Umkarton aufbewahren.
Nicht über 25 °C lagern.
Sie dürfen das Tierarzneimittel nach dem auf Faltschachtel und Euterinjektor nach „verw. bis“ angegebenen Datum nicht mehr anwenden. Das Verfalldatum bezieht sich auf den letzten Tag des Monats.
Besondere Vorsichtsmaßnahmen für die Entsorgung
Nicht aufgebrauchte Tierarzneimittel sind vorzugsweise bei Schadstoffsammelstellen abzugeben. Bei gemeinsamer Entsorgung mit dem Hausmüll ist sicherzustellen, dass kein missbräuchlicher Zugriff auf diese Abfälle erfolgen kann. Tierarzneimittel dürfen nicht mit dem Abwasser bzw. über die Kanalisation entsorgt werden. Diese Maßnahmen dienen dem Umweltschutz.
Fragen Sie Ihren Tierarzt oder Apotheker, wie nicht mehr benötigte Arzneimittel zu entsorgen sind.
Besondere Vorsichtsmaßnahmen für die Entsorgung von nicht verwendetem Arzneimittel oder von Abfallmaterialien, sofern erforderlich
Nicht aufgebrauchte Tierarzneimittel sind vorzugsweise bei Schadstoffsammelstellen abzugeben. Bei gemeinsamer Entsorgung mit dem Hausmüll ist sicherzustellen, dass kein missbräuchlicher Zugriff auf diese Abfälle erfolgen kann. Tierarzneimittel dürfen nicht mit dem Abwasser bzw. über die Kanalisation entsorgt werden.
Einstufung von Tierarzneimitteln
Tierarzneimittel, das der Verschreibungspflicht unterliegt.
Zulassungsnummern und Packungsgrößen
Zul.-Nr. 402205.00.00
Packungsgrößen:
4 Euterinjektoren und 4 Reinigungstücher
20 Euterinjektoren und 20 Reinigungstücher
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Datum der letzten Überarbeitung der Packungsbeilage
02/2023
Detaillierte Angaben zu diesem Tierarzneimittel sind in der Produktdatenbank der Europäischen Union verfügbar (https://medicines.health.europa.eu/veterinary).
Weitere Angaben
Cefapirin ist ein Cephalosporin der 1. Generation, das durch die Hemmung der Zellwandsynthese wirkt. Es wirkt bakterizid, hat eine zeitabhängige Wirkung und ein breites therapeutisches Wirkungsspektrum.
In vitro wurde eine Wirksamkeit gegen bekannte grampositive und gramnegative Bakterien einschließlich Escherichia coli, Staphylococcus aureus, Koagulase-negative Staphylokokken, Streptococcus dysgalactiae, Streptococcus agalactiae und Streptococcus uberis nachgewiesen.
Eine Übersicht der MHK50– und MHK90-Werte der häufigsten bakteriellen Mastitiserreger, die im Rahmen eines Resistenzmonitoring-Programmes (VetPath-Programm des Europäischen Zentrums für Studien zur Tiergesundheit (CEESA)) gesammelt wurden, findet sich in nachfolgender Tabelle (Die Daten zu Streptococcus agalactiae wurden während klinischer Studien im Zeitraum von 1984 bis 2005 erhoben):
| Isolierte Bakterienspezies | N | MHK50 (µg/ml) | MHK90 (µg/ml) |
| Staphylococcus aureus | 192 | 0,12 | 0,25 |
| Koagulase-negativeStaphylococci | 165 | 0,12 | 0,25 |
| Streptococcus uberis | 188 | 0,25 | 0,5 |
| Streptococcus dysgalactiae | 95 | 0,06 | 0,06 |
| Streptococcus agalactiae | 58 | 0,25 | 0,25 |
| Escherichia coli | 207 | 16 | >32 |
Während der letzten 10 Jahre wurde lediglich ein Anstieg des MHK90-Wertes für E.coli beobachtet.
Prednisolon hat eine entzündungshemmende Wirkung in der frühen und späten Phase einer Entzündung. Die intramammäre Anwendung von Prednisolon führt zu einer Abschwellung und folglich zu einer Verkleinerung des infizierten Euterviertels und fördert die Fiebersenkung bei erkrankten Tieren. Nach intramammärer Verabreichung des Tierarzneimittels werden Cefapirin und Prednisolon hauptsächlich mit der Milch beim Melkvorgang ausgeschieden. Die Resorption sowohl von Cefapirin als auch von Prednisolon ins Blut erfolgt schnell und nur begrenzt. Cefapirin als auch Prednisolon werden hauptsächlich mit dem Urin ausgeschieden.
Eine Übersicht zu den Konzentrationen von Cefapirin und Prednisolon in der Milch während der Behandlung befindet sich in der nachfolgenden Tabelle:
| Wirkstoff | Mittlere Wirkstoffkonzentration in der Milch in den auf die 1. Behandlung folgenden Gemelken | ||||
| 0 | 1. Gemelk | 2. Gemelk | 3. Gemelk | 4. Gemelk | |
| Cefapirin (µg/ml) | 0 | 27,0 ± 6,2 | 30,2 ± 7,9 | 40,0 ± 8,8 | 34,6 ± 6,5 |
| Prednisolon (ng/ml) | 0 | 182,0 ± 61,7 | 100,8 ± 51,0 | 283,7 ± 129,8 | 101,5 ± 38,8 |
Verschreibungspflichtig
